El tratamiento farmacológico de la insuficiencia mitral descansa en la administración de digoxina, diuréticos y vasodilatadores. La digoxina es útil en ventrículos dilatados y con contractilidad deprimida, especialmente cuando existe fibrilación auricular. Los diuréticos ayudan a tratar la congestión pulmonar y a reducir los síntomas derivados. Los vasodilatadores arteriales (inhibidores de la enzima conversora de angiotensina, hidralazina) reducen las resistencias arteriales y facilitan que el flujo que el ventrículo izquierdo eyecta en la sístole se dirija hacia la aorta más que hacia la aurícula izquierda.
En casos de insuficiencia mitral aguda (como la que sucede, por ejemplo, por rotura de parte del aparato subvalvular en un infarto agudo de miocardio) la poca distensibilidad de una aurícula que no ha tenido tiempo de adaptarse a la sobrecarga brusca de volumen hace que las presiones aumenten mucho y se produzca edema agudo de pulmón. En esta situación los vasodilatadores deben administrarse por vía intravenosa y en el contexto de una unidad de cuidados intensivos, siendo el nitroprusiato sódico una buena opción. Si esto no es suficiente, puede requerirse la implantación de un balón de contrapulsación intraaórtico.

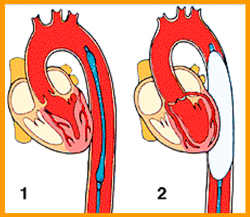 El balón de contrapulsación, que se hincha de forma sincronizada con el latido cardiaco, se encuentra en el extremo de un catéter que se sitúa en la aorta torácica descendente. El volumen de hinchado es de 30-50 ml y emplea helio como gas inerte. El catéter se inserta a través de la arteria femoral, bien mediante la técnica percutánea de Seldinger, bien mediante abordaje directo de la arteria. La colocación correcta, que requiere control radiológico, se alcanza cuando el extremo del catéter está situado justo por debajo del nacimiento de la arteria subclavia izquierda.
El balón de contrapulsación, que se hincha de forma sincronizada con el latido cardiaco, se encuentra en el extremo de un catéter que se sitúa en la aorta torácica descendente. El volumen de hinchado es de 30-50 ml y emplea helio como gas inerte. El catéter se inserta a través de la arteria femoral, bien mediante la técnica percutánea de Seldinger, bien mediante abordaje directo de la arteria. La colocación correcta, que requiere control radiológico, se alcanza cuando el extremo del catéter está situado justo por debajo del nacimiento de la arteria subclavia izquierda.
El hinchado del balón se realiza coincidiendo con la onda dícrota del pulso aórtico y se deshincha justo antes de la sístole. Los beneficios hemodinámicos del contrapulsador intraaórtico se basan en una reducción de la postcarga aórtica, al deshincharse bruscamente al comienzo de la sístole, y una mejoría de la perfusión coronaria, al aumentar el hinchado del globo la presión diastólica aórtica. Por ello este dispositivo está particularmente indicado en situaciones de insuficiencia cardiaca-bajo gasto secundario a isquemia miocárdica (shock cardiogénico, complicaciones mecánicas del infarto agudo de miocardio, como rotura del tabique interventricular o insuficiencia mitral aguda, síndrome de bajo gasto postcirculación extracorpórea, etc.). También se utiliza como respaldo en casos de angioplastia o coronariografía de alto riesgo.
Es evidente que esta técnica está contraindicada en casos de insuficiencia o disección aórtica, así como en la persistencia del conducto arterioso. Las principales complicaciones de esta técnica son la isquemia de las extremidades y la sepsis, cuyo riesgo aumenta con el tiempo, por lo que la contrapulsación intraaórtica se ve limitada a unos cuantos días, tiempo que debe bastar para solucionar, por medios médicos o quirúrgicos, la situación que dio origen a su inserción.
El tratamiento médico está reservado a pacientes con buena función ventricular y que, gracias a este procedimiento, se mantienen en una situación asintomática o con escasos síntomas; o bien a enfermos en que el riesgo de la intervención quirúrgica es inaceptable.
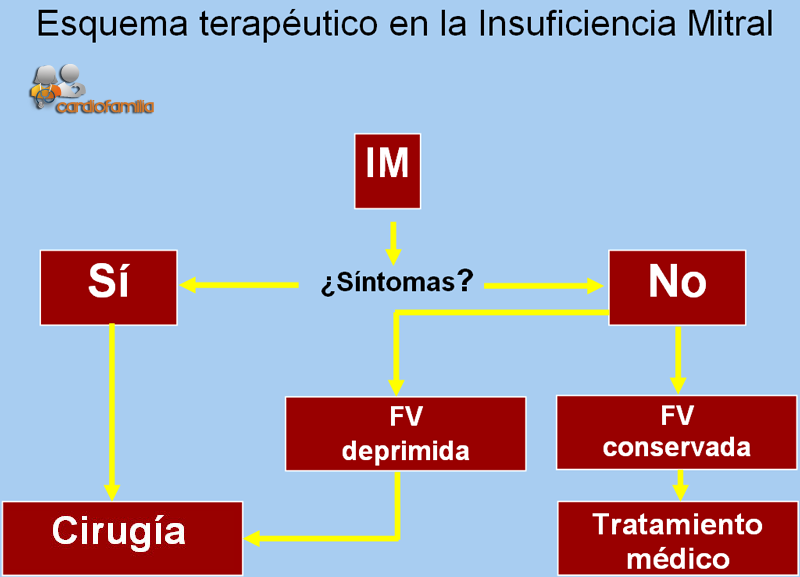
Esa es también la razón de que se escoja como indicación de depresión de la función ventricular una cifra (0,6 de fracción de eyección) que parece bastante normal. Aunque se suele considerar que la fracción de eyección es una medida bastante aceptable de la contractilidad, en realidad depende bastante de la postcarga, de forma que aumenta cuando ésta es baja. Por eso en la insuficiencia mitral, en que la postcarga es baja, sería de esperar una fracción de eyección aumentada; el hecho de encontrar valores normales ya es «anormal».
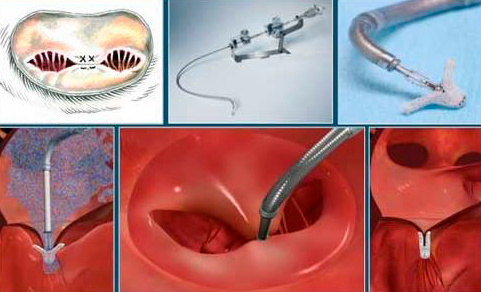
En la actualidad, y en manos de equipos experimentados, la baja mortalidad quirúrgica y los excelentes resultados funcionales de las distintas técnicas de reparación valvular, hacen que en muchos casos en que esta técnica es factible se tienda a adelantar la intervención. En casos muy seleccionados se está comenzando a aplicar técnicas percutáneas, por medio de cateterismo (sin cirugía) para reducir la cuantía de la regurgitación (Mitra Clip).
En el caso de la insuficiencia mitral secundaria, la situación es distinta. Puesto que en estos casos la función ventricular suele estar deprimida, con frecuencia en grado severo, la cirugía comporta un elevado riesgo, por lo que hay que considerarla si el paciente se va a intervenir de revascularización coronaria, o si se considera que puede conseguirse una reparación valvular con bajo riesgo. En esta situación puede considerarse una técnica percutánea (Mitra Clip), siempre en manos experimentadas.
Esquema del manejo de un paciente con sospecha de insuficiencia mitral
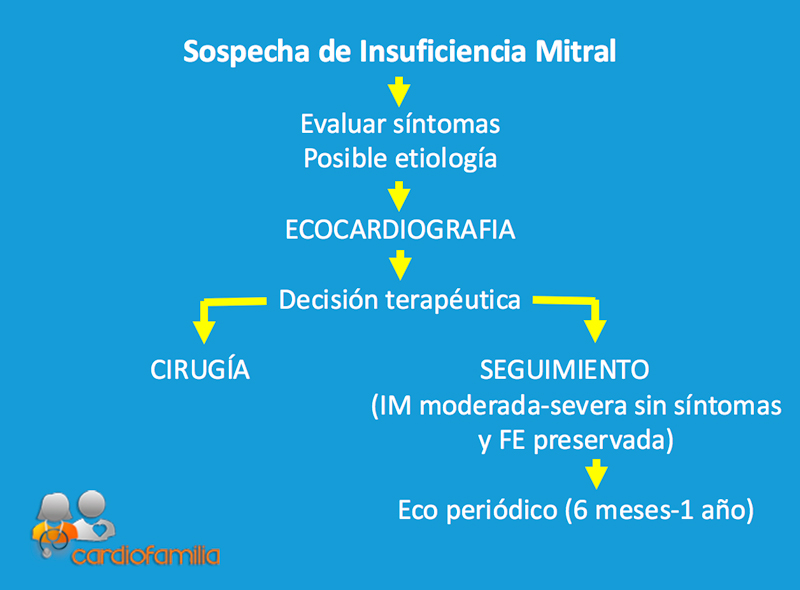
Esquema de manejo del paciente con sospecha de insuficiencia mitral en Atención Primaria. Frente a un paciente con sospecha de IM, debe evaluarse la presencia de sintomatología, la posible etiología y la existencia de fibrilación auricular. Una vez hecho esto, el diagnóstico y la posible indicación terapéutica depende de los hallazgos ecocardiográficos. Según estos, se adopta la decisión de intervenir para reparar o sustituir la válvula, o bien realizar un seguimiento. Los pacientes seleccionados para este último caso son los que tienen una IM moderada-severa, no presentan síntomas ni depresión de función ventricular. El seguimiento requiere evaluación periódica de los síntomas y ecocardiograma seriado.